Artículo Original
Manejo de la cianosis en pacientes con circulación tipo Fontan-Kreutzer
José L Alonso, Victoria Lafuente, Rosalín Ramírez Aguilar, José Pibernus, Alberto Sciegata, Francisco Comas, Horacio Faella, Horacio Capelli, Alejandra Villa, Mariela Mouratian
Revista Argentina de Cardioangiología Intervencionista 2013;(02): 0092-0098 | Doi: 10.30567/RACI/201302/0092-0098
Existen múltiples causas de cianosis en pacientes con cirugía Fontan-Kreutzer y sus modificaciones. Evaluaremos los tipos de comunicación de derecha a izquierda y la posibilidad de su tratamiento percutáneo.
Entre mayo de 1998 y junio de 2012, se realizaron 87 cateterismos consecutivos en 85 pacientes con cirugía tipo bypass de ventrículo derecho y cianosis, con edad X: 7±4,3 años y peso X: 19,5±13,7 kg.
Cuando la cianosis fue causada por comunicaciones pasibles de cierre, se procedió al tratamiento percutáneo de aquellas empleando distintas clases de dispositivos.
Los diferentes tipos de comunicaciones tratadas fueron: fenestraciones (n=47) (dos pacientes necesitaron dos procedimientos por cortocircuito residual), comunicaciones venovenosas (n=29) (26 entre venas sistémicas y venas pulmonares o la aurícula sistémica y 3 vena cava superior izquierda), fístulas arteriovenosas pulmonares (n=4), que se encontraron especialmente en pacientes con cirugía de Kawashima.
En 5 pacientes fueron tratadas múltiples comunicaciones.
Se obtuvieron incrementos en la saturación, de X: 84,96±6% a X: 93,96±4,4% (p<0,000001), con aumentos de presiones de X: 12,7±2,6 mmHg a X: 13,7±2,8 mmHg, con un rango entre 9 y 19 mmHg.
No hubo complicaciones de importancia.
Existen diferentes tipos de comunicaciones de derecha a izquierda en pacientes con cirugía Fontan Kreutzer que provocan cianosis y deterioran su funcionamiento. Estas comunicaciones, algunas creadas quirúrgicamente y otras por anormal desarrollo, pueden en su mayoría tratarse en forma percutánea empleando distintas estrategias y dispositivos.
Palabras clave: cirugÃa Fontan-Kreutzer, cianosis.
There are multiple causes of cyanosis in patients with Fontan-Kreutzer surgery. The purpose of this paper is to evaluate the types of right to left shunts, and the possibility of percutaneous treatment of them.
Between May 1998 and June 2012, 87 consecutive catheterizations were performed in 85 patients with bypass surgery of the right ventricle and cyanosis, aged X: 7±4.3 years and weight X: 19.5±13.7 kg.
When cyanosis was caused by communications amenable of closure, percutaneous treatment was carried out using diferent kinds of devices.
The different types of communications treated were: fenestration (n=47), two patients required two procedures for residual shunt in it, venovenous communications (n=29), 26 between systemic veins and pulmonary veins or the systemic atrium and 3 left superior vena cava, pulmonary arteriovenous fistulas (n=4), which is found especially in patients with Kawashima surgery.
In 5 patients multiple communications were treated.
Saturation increases from X: 84.96±6% to X: 93.96±4.4%, p <0.000001, and pressure from X: 12.7±2.6 mmHg to 13.7±2.8 mmHg with a 9 to 19 mmHg range.
There were no significant complications.
Several different types of communications from right to left in patients with Fontan Kreutzer surgery cause cyanosis and deteriorate its performance. These communications, some created surgically and others by abnormal development, can be mostly percutaneously treated, using different strategies and devices.
Keywords: Fontan-Kreutzer surgery, cyanosis.
Los autores declaran no poseer conflictos de intereses.
Fuente de información Colegio Argentino de Cardioangiólogos Intervencionistas. Para solicitudes de reimpresión a Revista Argentina de Cardioangiología intervencionista hacer click aquí.
Recibido 2013-05-03 | Aceptado 2013-05-16 | Publicado

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-SinDerivar 4.0 Internacional.



Introducción
Existen múltiples causas de cianosis en los pacientes con circulación tipo Fontan-Kreutzer. De ellas, la más común es la existencia de una fenestración creada quirúrgicamente; otras se deben a anormal desarrollo en la evolución, como múltiples comunicaciones entre el circuito pulmonar y las venas pulmonares y/o la aurícula sistémica y fístulas arteriovenosas pulmonares. El desarrollo de diferentes dispositivos permite el tratamiento de la mayoría de estas patologías de difícil abordaje quirúrgico. En este artículo describiremos nuestra experiencia en el tratamiento percutáneo empleando diferentes tipos de dispositivos.1-3
Material y método
En nuestro grupo quirúrgico sólo se dejaba fenestración cuando los pacientes presentaban factores de riesgo (aquellos que no cumplían estrictamente con todos los criterios de Choussat). A partir de los últimos años, se comenzó a dejar fenestración en todos los pacientes.4
Todos fueron evaluados clínicamente con saturometría, presión arterial, Rx Tx, ECG y ecocardiograma transtorácico; la indicación de cateterismo en este subgrupo de pacientes con fisiología univentricular fue el descenso progresivo de la saturación a menos de 90%. Los pacientes de nuestra serie se encontraban en tratamiento con AAS 3/5 mg/kg día, y dos que presentaban antecedentes de accidente cerebrovascular se encontraban anticoagulados.
A los pacientes y sus familiares responsables se les explicó la naturaleza del procedimiento y se obtuvo el consentimiento informado.
Todos los procedimientos se realizaron bajo anestesia general y por técnica de Seldinger; el abordaje fue por vena femoral y yugular interna en prácticamente todos los cateterismos. Como abordaje alternativo en pacientes con múltiples intervenciones y malos accesos vasculares, y en algunos con interrupción de vena cava inferior y cirugía de Kawashima, se utilizó la vía transhepática. En los casos de abordaje transhepático, la punción se realizó con guía ecográfica y aguja de Chiba, aunque puede realizarse sin guía ecográfica (Figura 1). Se administró heparina a una dosis de 100 UI/kg en todos los pacientes excepto en aquellos que se encontraban previamente anticoagulados.
Se realizaron angiografías selectivas en la vena cava inferior, el conducto extracardíaco, las ramas pulmonares, la vena cava superior ya sea derecha y o izquierda y en ambas venas yugulares en busca de comunicaciones de derecha a izquierda.
Fueron investigados los gradientes de presión entre las distintas cavidades y también fue evaluada la existencia de colaterales aortopulmonares antes de iniciar cualquier tipo de procedimiento terapéutico.
Cuando existían estenosis involucradas en el circuito pulmonar y/o colaterales aortopulmonares que pudieran ocasionar aumentos en la presión del circuito pulmonar, ambas patologías fueron tratadas antes de realizar oclusión de las conexiones de derecha a izquierda (Figura 2).
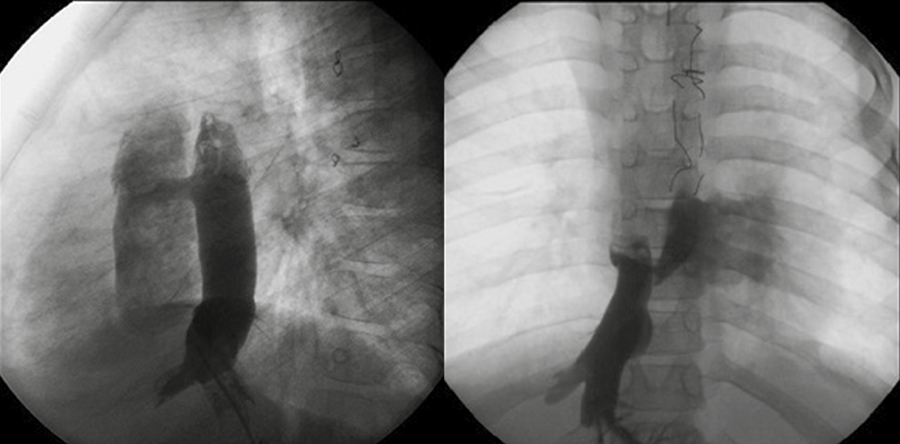
Cuando existían comunicaciones anormales entre el sistema venoso y las venas pulmonares o la aurícula sistémica, se realizaron angiografías selectivas en distintas incidencias para determinar con mayor precisión la anatomía, trayecto, diámetro y longitud, para la elección del tipo de dispositivo (Figura 3).
Para la embolización de las colaterales venovenosas se emplearon coils de Gianturco, dispositivos tipo Amplatzer (vascular plug, oclusor de ductus) y ocasionalmente microcoils, seleccionando un tamaño entre un 30 y 50% mayor que el diámetro del vaso.5
Con guías específicas de acuerdo al material embolígeno se cateterizó selectivamente el vaso a ocluir, y con catéteres específicos según el caso se posicionó el dispositivo oclusor (tipo coronaria derecha, Envoy, liberador de dispositivo Amplatzer, de Nit-Occlud) y previo a la liberación por una llave en Y se verificó la adecuada ubicación en los casos en que fue posible.
A los 10 minutos se realizaron angiografías de control y eventualmente se colocaron más dispositivos para lograr la oclusión deseada.
Las fístulas arteriovenosas pulmonares fueron encontradas especialmente en pacientes con operación de Kawashima; se realizaron angiografías selectivas en ambas ramas de la arteria pulmonar y cuando las fístulas eran mayores (de un tamaño que ameritaban tratamiento) se hicieron angiografías selectivas y se ocluyeron con dispositivos empleando el mismo criterio que en las colaterales venosas. Las fístulas arteriovenosas pulmonares muy pequeñas y múltiples (microfístulas) no pudieron ser embolizadas.6
En pacientes con fenestraciones se realizó test de oclusión con catéter Berman Angiográfico Arrow NR (catéter angiográfico con balón, con orificios que permiten tomar la presión en el circuito pulmonar), se tomaron presiones y oximetrías con la fenestración abierta y cerrada con el balón (Figura 4). En aquellos pacientes con presión en el circuito pulmonar menor a 18 mmHg durante la oclusión se realizó el cierre, cuando la presión fue de 18 mmHg o más se realizó el cierre cuando la presión no se elevó más de 1 mmHg.7,8
Luego del cierre se tomaron presiones y oximetrías.
Los dispositivos utilizados fueron:
• 26 dispositivos para cierre de CIA Amplatzer, con tamaños entre 4 y 8 mm.
• 3 de CIA cribiforme Amplatzer de 25 mm.
• 7 de foramen oval de Amplatzer 5 de 15 mm, 2 de 20 mm y 1 de 25 mm.
• 1 de ductus Amplatzer 6/4.
• 2 Atriasept de 25 mm.
• 8 Helex 5 de 15 mm, 2 de 20 mm y 1 de 25 mm.
• 2 stents recubiertos.
Cuando la fenestración fue cerrada con dispositivos de anclaje en el defecto, se introdujo una guía de extrasoporte a través dela fenestración y luego se colocaron los dispositivos de manera habitual para cada tipo de prótesis. En el caso de los stents, se evaluó el parte quirúrgico para conocer el tamaño nominal del tubo y se realizaron angiografías para confirmar el tamaño del mismo; con una guía de extrasoporte en la arteria pulmonar se introdujo una camisa transeptal adecuada y a través de ella se posicionó el stent.9
En los pacientes que presentaron múltiples comunicaciones, se fueron ocluyendo y tomando saturometría y presión luego del cierre de cada una de ellas, y al llegar a los 18 mmHg de presión en el circuito pulmonar se dieron por finalizadas las oclusiones.
Resultados
Entre mayo de 1998 y junio de 2012 se realizaron 87 cateterismos consecutivos en 85 pacientes con cirugía tipo bypass de ventrículo derecho y cianosis, con mediana de edad de 7±4,3 años y mediana de peso de 19,5±13,7 kg.
Los valores de saturación y las presiones en todo el circuito pulmonar están reflejadas en las Tabla 1. No se logró saturación superior a 90% en pacientes con fistulas arteriovenosas pulmonares asociadas a cirugía de Kawashima.
La presión venosa en el circuito pulmonar aumentó de 12,7±2,6 mmHg a 13,7± 2,8 mmHg, con un rango entre 9 y 19 mmHg. Al mismo tiempo, hubo un incremento de la saturación de 84,96±6% a 93,96±4,4%, p <0,000001, con un rango de 80 a 100%.
Fueron ocluidas: 47 fenestraciones, 29 colaterales venovenosas o venoatriales, 4 fistulas AVP y en 5 pacientes, múltiples comunicaciones.
En cuanto a los pacientes con fenestración, dos necesitaron un segundo procedimiento. En uno de ellos, con dispositivo Helex se abrió el disco derecho y se colocó un stent recubierto, que fue impactado en el tubo extracardíaco ocluyendo el defecto y dejando libre el conducto. El segundo paciente tenía implantado un dispositivo de CIA cribiforme que quedó con saturación de 93% pero con cortocircuito residual inmediato, pese a lo cual en el seguimiento evolucionó con insaturación; en un segundo procedimiento se le colocó un stent recubierto sobre la misma lográndose oclusión total y saturación de 96%.10
En 5 pacientes fueron ocluidas múltiples conexiones.
No hubo complicaciones de importancia.
En dos pacientes, la prótesis tuvo que ser retirada y en el mismo procedimiento fue colocada otra en forma efectiva. La primera, un dispositivo Solysafe no quedaba bien configurado y fue retirado; la segunda, un dispositivo Amplatzer de CIA se configuró con forma de cobra y fue retirado (Figura 5). Ambos fueron reemplazados por otro dispositivo Amplatzer de CIA.
Discusión
En la evolución de los pacientes con cirugía de Fontan-Kreutzer los eventos son frecuentes, y dentro de ellos la cianosis es una complicación habitual.
En nuestra serie, la causa más común de comunicación de derecha a izquierda son las fenestraciones, dato que coincide con lo descripto en la bibliografía.
La indicación de dejar fenestración es variable de institución a institución. En nuestro hospital inicialmente la fenestración se indicaba a aquellos pacientes que no cumplían estrictamente con los criterios de Choussat, es decir, pacientes con alto riesgo para cirugías de tipo Fontan Kreutzer, pero en los últimos años se ha extendido la indicación a todos los pacientes debido a la observación de una recuperación posquirúrgica más rápida y con menos complicaciones en aquellos pacientes fenestrados.11,12
Asimismo, el cierre de la fenestración en el seguimiento de los pacientes con cirugías de tipo univentricular es discutido. Sólo se evalúa la posibilidad de cierre en aquellos pacientes en quienes la saturación desciende por debajo de 90% (estos pacientes pueden tener profunda cianosis durante el ejercicio) o en quienes las ventajas teóricas de una mejor saturación superan la desventaja de una pequeña disminución en el volumen minuto cardíaco y de un pequeño aumento en la presión venosa.13,14
Los riesgos de embolia paradójica, que ocurrió en 2 de nuestros pacientes, también desaparecen con el cierre de la comunicación.
Nuestro grupo realiza test de oclusión en todos los pacientes antes de decidir el cierre de la fenestración, el nivel de corte para no cerrar la fenestración fue un ascenso de la presión venosa media a 19 mmHg o más, a diferencia de la sugerencia de Bridges y cols., que emplean un aumento a 16 mmHg o más para no cerrar la fenestración, Pinkala y cols., que no la cierran cuando la presión venosa aumenta más de 4 mmHg y similar al de Masura y cols. que recomiendan cerrarla sólo con presiones inferiores a 18 y dejarla permeable cuando con el test de oclusión la presión asciende a 20 mmHg o más (Figura 6).
En nuestra serie no tuvimos derrame en ningún paciente, a diferencia de aquellos grupos que tomaron como corte 20 mmHg donde el 50% de los pacientes con esta presión en el circuito pulmonar presentaron esta complicación.
Es importante destacar que es necesario realizar un seguimiento a largo plazo luego del cierre de las fenestraciones.
Los resultados obtenidos por nuestro grupo muestran que es un procedimiento seguro, efectivo y repetible, y que puede realizarse con distintos tipos de dispositivos, obteniéndose resultados muy buenos en forma inmediata y que se mantienen en el seguimiento a corto plazo, confirmando los hallazgos reportados por Pinkala y cols.15,16
En relación con los diferentes tipos de dispositivos utilizados, no hubo diferencias en los resultados ni en las complicaciones. Solamente vale un comentario con relación al dispositivo Solysafe, que no pudo ser bien configurado; era el primero de estos dispositivos que tratamos de colocar y luego, por otros motivos, fue retirado del mercado.
En relación con los stents recubiertos, tendrían hipotéticamente la ventaja de tener menos material metálico y celdas grandes donde la malla de Goretex NR podría ser perforada, si fuera necesario en el seguimiento hacer una nueva fenestración. La posible desventaja sería su estructura con Goretex en relación con la formación de trombos, pero, como fue comentado en párrafos anteriores, todos los pacientes con anatomía y circulación univentricular son antiagregados y algunos anticoagulados, por lo que pensamos que cuando la anatomía del conducto lo permite pueden ser una alternativa en el tratamiento. No obstante, mayor experiencia es necesaria para afirmarlo con certeza.
La segunda causa de cianosis son las colaterales venosas. La disminución de la saturación en forma lenta y progresiva sugiere el desarrollo de colaterales venosas con la aurícula sistémica o con las venas pulmonares (Figura 7).
En este subgrupo de pacientes, las presiones venosas fueron bajas y siempre pudieron ser embolizadas. Sólo no fueron ocluidas cuando estaban asociadas a fenestraciones que al ser ocluidas provocaban un aumento en la presión venosa a 18 mmHg. Siempre que hubo asociación de defectos, fenestración más colaterales, se evaluó el cierre en primer término de la fenestración, que en nuestra experiencia es la que ocasiona mayor cortocircuito de derecha a izquierda, y se valoró el cierre de las colaterales venosas de acuerdo a la presión venosa con la fenestración cerrada: si esta subía a 18 mmHg, no se ocluyeron las colaterales venosas, asumiendo que podrían funcionar en el futuro como escape por dilatación progresiva de las mismas y que eventualmente podrían ser embolizadas en el futuro. Si al realizar el test de oclusión de la fenestración la presión subía a 18 mmHg o más, se comenzó embolizando las colaterales venovenosas evaluando las presiones y saturación luego del cierre de cada una.
En 3 pacientes se evidenció persistencia de vena cava izquierda en seno coronario y/o aurícula sistémica que no habían sido observadas en el cateterismo previo al Fontan; creemos que previamente eran hipoplásicas y que se reabrieron por aumento de la presión venosa luego de completar la corrección quirúrgica (Fontan-Kreutzer) provocando cianosis importante.
Pequeñas y múltiples fístulas arteriovenosas pulmonares fueron halladas en 4 pacientes de nuestra serie, y fueron el subgrupo con cianosis más importante, todas en pacientes con operación de Kawashima, en tres de ellos se encontraron múltiples fístulas, algunas pudieron ser embolizadas mejorando parcialmente la saturación. En los pacientes con cirugía de Kawashima, la incorporación precoz del flujo hepático prevendría la formación de fístulas.
Conclusiones
Además de las fenestraciones, una gran variedad de comunicaciones pueden causar cianosis en pacientes con circulación tipo Fontan-Kreutzer. La progresiva disminución de la saturación es sugestiva del desarrollo de estas comunicaciones de derecha a izquierda, ya sean colaterales o fistulas arteriovenosas pulmonares.
Estas comunicaciones son en su gran mayoría pasibles del cierre por cateterismo intervencionista empleando diferentes tipos de dispositivos, y con todos ellos se obtenien buenos resultados. Es importante realizar seguimiento alejado de estos pacientes.
-
J. Kreutzer. Cateterismo intervencionista en pacientes con circulación tipo Fontan. Rev Argent Cardiol 1996;64(4):379-388.
-
Masura J, Borodacova L, Tittel P, Berden P, Podnar T. Percutaneous management of cyanosis in Fontan patients using Amplatzer occluders. Catheter Cardiovasc Interv 2008;71:843-849.
-
Jeong SI, Huh J, Lee HJ, Yang JH, Jun TG, Kang IS. Closure of conduit fenetratio after Fontan procedure using Amplatzer vascular plug: comparison with detachable coil. Pediatr Cardiol 2010;31:44-49.
-
Bridges ND, Mayer JE, Lock JE, Jonas RA, Hanley FL, Keane JF, Perry SB, Castaneda AR. Effect of baffle fenestration on outcome of the modiï¬ed Fontan operation. Circulation 1992;86:1762-1769.
-
Hill SL, Hijazi ZM, Hellenbrand WE, Cheatham JP. Evaluation of the Amplatzer vascular plug for embolization of peripheral vascular malformations associated with congenital heart disease. Catheter Cardiovasc Interv 2006;67:113-119.
-
Alonso J, Sciegata A, Jelmitzky L, Lipsich J, Faella H. Tratamiento por cateterismo de malformaciones arteriovenosas pulmonares. Medicina Infantil 2001;VIII:13-17.
-
Senzaki H, Naito C, Masutani S, Nogaki M, Ohono A, Kobayashi J, Sasaki N, Asano H, Shunei K, Yokote Y, Kobayashi T. Hemodynamic evaluation for closing interatrial communication after fenestrated Fontan operation. J Thorac Cardiovasc Surg 2001;121:1200-1202.
-
Bridges ND, Lock JE, Mayer JE, Burnett J, Castaneda AR. Cardiac catheterization and test occlusion of the interatrial communication after the fenestrated Fontan operation. J Am Coll Cardiol 1995;25:1712-1717.
-
Butera G, Piazza L, Chessa M, Abella R, Bussadori C, Negura D, Carminati M. Covered stents in patients with congenital heart defects. Catheter Cardiovasc Interv 2006;67:466-472.
-
Hijazi ZM, Ruiz CE, Patel H, Cao QL, Dorros G. Catheter therapy for Fontan baffle obstruction and leak using an endovascular covered stent. Cathet Cardiovasc Diagn 1998;45:158-161.
-
Bridges ND, Lock JE, Castaneda AR.Baffle fenestration with subsequent transcatheter closure. Modification of the Fontan operation for patients at increased risk. Circulation 1990;82:1681-1689.
-
Goff DA, Blume ED, Gauvreau K, Mayer JE, Lock JE, Jenkins KJ. Clinical outcome of fenestrated Fontan patients after closure. The first 10 years. Circulation 2000;102:2094-2099.
-
Hijazi ZM, Fahey JT, Kleinman CS, Kopf GS, Hellenbrand WE. Hemodynamic evaluation before and after closure of fenestrated Fontan. An acute study of changes in oxygen delivery. Circulation 1992;86:196-202.
-
Cowley CG, Badran S, Gaffney D, Rocchini AP, Lloyd TR. Transcatheter closure of Fontan fenestrations using the Amplatzer septal occluder: initial experience and follow-up. Catheter Cardiovasc Interv 2000;51:301-304.
-
Pihkala J, Yazaki S, Mehta R, Lee KJ, Chaturvedi R, McCrindle BW, Van Arsdell G, Benson LN. Feasibility and clinical impact of transcatheter closure of interatrial communications after a fenestrated Fontan procedure: medium-term outcomes. Catheter Cardiovasc Interv 2007;69:1007-1014.
-
Meraji SM, Davari PN, Aarabi MY, Shahmohammadi AA, Mortezaeian H, Emamzadegan R. Transcatheter closure of fenestration after modified Fontan operation in children. J Tehran Heart Cent 2008;3(1):39-42.
José L Alonso
Servicio de Hemodinamia, Hospital Nacional de Pediatría “Prof. Dr. Juan P. Garrahan”. CABA, Argentina.
Victoria Lafuente
Servicio de Hemodinamia, Hospital Nacional de Pediatría “Prof. Dr. Juan P. Garrahan”. CABA, Argentina.
Rosalín Ramírez Aguilar
Servicio de Hemodinamia, Hospital Nacional de Pediatría “Prof. Dr. Juan P. Garrahan”. CABA, Argentina.
José Pibernus
Servicio de Hemodinamia, Hospital Nacional de Pediatría “Prof. Dr. Juan P. Garrahan”. CABA, Argentina.
Alberto Sciegata
Servicio de Hemodinamia, Hospital Nacional de Pediatría “Prof. Dr. Juan P. Garrahan”. CABA, Argentina.
Francisco Comas
Servicio de Hemodinamia, Hospital Nacional de Pediatría “Prof. Dr. Juan P. Garrahan”. CABA, Argentina.
Horacio Faella
Servicio de Hemodinamia, Hospital Nacional de Pediatría “Prof. Dr. Juan P. Garrahan”. CABA, Argentina.
Horacio Capelli
Servicio de Hemodinamia, Hospital Nacional de Pediatría “Prof. Dr. Juan P. Garrahan”. CABA, Argentina.
Alejandra Villa
Servicio de Hemodinamia, Hospital Nacional de Pediatría “Prof. Dr. Juan P. Garrahan”. CABA, Argentina.
Mariela Mouratian
Servicio de Hemodinamia, Hospital Nacional de Pediatría “Prof. Dr. Juan P. Garrahan”. CABA, Argentina.
Autor correspondencia
José L Alonso
Servicio de Hemodinamia, Hospital Nacional de PediatrÃa “Prof. Dr. Juan P. Garrahanâ€. CABA, Argentina.
Correo electrónico: Tel: 46292879 | Tel: 54 1164860883 | alonsojl@infovia.com.ar
Para descargar el PDF del artículo
Manejo de la cianosis en pacientes con circulación tipo Fontan-Kreutzer
![]() Haga click aquí
Haga click aquí
Para descargar el PDF de la revista completa
Revista Argentina de Cardioangiología intervencionista, Volumen Año 2013 Num 02
Revista Argentina de Cardioangiología intervencionista
Número 02 | Volumen
3 | Año 2013
Orígenes, desarrollo y contribucio...
Alberto Rodríguez Coronel
Cardiología Pediátrica en nuestra...
Alfredo Eduardo Rodríguez
Percutaneous pulmonary valve implan...
Jacqueline Kreutzer
Manejo de la cianosis en pacientes ...
José L Alonso y cols.
Cierre de ductus por cateterismo co...
Jesús Damsky Barbosa y cols.
Cierre percutáneo de ductus arteri...
María Celeste Carrero y cols.
Acceso venoso transhepático: una a...
Alejandro R Peirone y cols.
Hemoptisis por estenosis congénita...
JL Pibernus y cols.
Endocarditis infecciosa poscierre d...
Luis Trentacoste y cols.
Coartación de aorta. Fractura alej...
Jesús Damsky Barbosa y cols.
Etiquetas
cirugÃa Fontan-Kreutzer, cianosis
Tags
Fontan-Kreutzer surgery, cyanosis
Manejo de la cianosis en pacientes con circulación tipo Fontan-Kreutzer
Autores
José L Alonso, Victoria Lafuente, Rosalín Ramírez Aguilar, José Pibernus, Alberto Sciegata, Francisco Comas, Horacio Faella, Horacio Capelli, Alejandra Villa, Mariela Mouratian
Publicación
Revista Argentina de Cardioangiología intervencionista
Editor
Colegio Argentino de Cardioangiólogos Intervencionistas
Fecha de publicación
2013-06-30
Registro de propiedad intelectual
© Colegio Argentino de Cardioangiólogos Intervencionistas